新冠病毒感染防治新阶段、新思考——益生菌在新冠病毒感染防治中的新探索
2022年12月7日,国务院应对新型冠状病毒肺炎疫情联防联控机制综合组公布了《关于进一步优化落实新冠肺炎疫情防控措施的通知》(简称“新十条”),“新十条“的公布意味着我国新冠病毒感染防治进入新阶段。短期内,新冠病毒感染人数将大幅增加,而伴随着感染高峰的到来及潜在的高危人群进展为重型及危重型风险,新冠病毒感染者的治疗仍将面临较大的挑战。在新形势下,有必要重新思考新冠病毒感染的综合治疗措施。除最常见的呼吸道症状外,新冠病毒感染后还会引发消化道症状在内的多系统疾病临床表现。而益生菌在新冠病毒感染治疗中具有不容忽视的重要应用价值。

一、新数据:新冠病毒感染将会导致多系统损害,消化道症状不容忽视
新冠病毒通过与血管紧张素转换酶 2( ACE-2) 结合而进入细胞内进而感染全身,即ACE-2在新冠病毒传播和病情进展过程中发挥着重要的作用。基础研究显示,ACE-2在食管上皮、回肠和结肠的吸收性肠上皮细胞中均有高表达。ACE-2高表达器官更易受到新冠病毒侵袭。临床研究显示,新冠病毒感染者胃肠道症状较为常见,其中腹泻症状更是高达7.4%~12.5%。
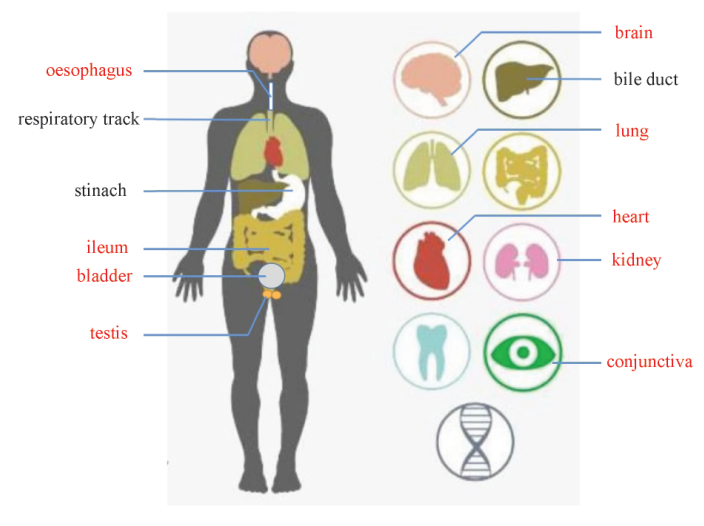
图1 ACE-2在人体的器官分布示意图
二、新发现:新冠病毒感染导致胃肠道症状/肠道菌群紊乱机制探究
新冠病毒对ACE-2受体存在选择性,其入侵过程需通过黏膜特异性II型跨膜丝氨酸蛋白酶(TMPRSS4和TMPRSS2)的介导。ACE-2和TMPRSS4以及TMPRSS2在肠上皮细胞中均呈高表达,介导了新冠病毒刺突蛋白(spike protein)与细胞的融合,促进了病毒的感染。肺组织受损后,病毒播散至全身,通过血循环和淋巴系统侵入肠道,对ACE-2高表达的小肠上皮细胞造成损害。病毒表面的突剌蛋白和ACE-2受体结合后侵入宿主细胞内,抑制ACE-2的表达。致使肠道中中性氨基酸转运蛋白B0AT1表达水平明显下降,导致小肠mTOR信号通路受到抑制,减少了小肠Paneth细胞中抗菌肽的分泌,导致肠道菌群的构成发生改变;另外病毒感染诱导的大量促炎细胞因子能够破坏肠道上皮的完整性,导致炎症和肠道菌群失调。
新冠病毒感染患者的肠道菌群发育不良,乳酸菌和双歧杆菌水平下降,粪芽孢菌属的丰度与疾病严重程度呈正相关,而粪杆菌属的丰度与疾病严重程度呈负相关。与健康人群相比,新冠病毒感染者的菌群多样性显著降低,条件致病菌如链球菌、罗氏菌、细根霉和放线菌的相对丰度显著升高,而有益共生菌的相对丰度较低。
新冠病毒感染者肠道菌群失调的另一原因可能是大量抗生素的使用。因为肺炎持续期间常伴有各种机会性感染。据调查,有多达58%~71%的患者在新冠肺炎治疗期间接受了抗生素治疗由于肠道细菌对抗生素的敏感性差异。抗生素使用极易诱发肠道菌群失调。增加对新感染和炎症性疾病的敏感性,同时易引起抗生素相关性腹泻。
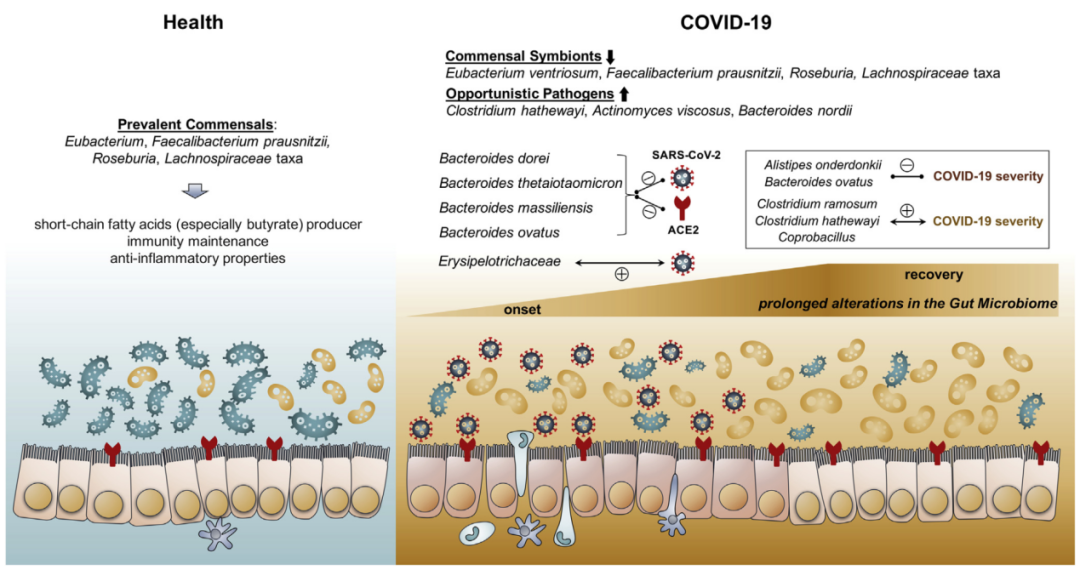
图2 健康人员与新冠病毒感染者肠道微生物菌群改变
新冠病毒同样可导致胃肠道细胞直接受损,引发相应症状。新冠病毒与胃肠道丰富表达的受体—ACE-2结合后进入肠道内皮细胞,病毒复制增加,导致胃肠道炎性反应、吸收异常、肠道分泌异常,并可导致肠道神经系统激活,从而出现腹泻、腹部疼痛等症状。
新冠病毒在胃肠道内的大量增殖,分泌大量细胞因子及趋化因子,诱发“细胞因子风暴。
当 IL-1β 、TNF-α 等细胞因子过度释放形成“细胞因子风暴”时,会造成过强的免疫反应,增加脓毒血症、急性呼吸窘迫综合征、多器官功能衰竭发生风险。

图3 新冠病毒感染导致胃肠道功能损伤/肠道菌群紊乱机制
三、新观点:肠道菌群紊乱影响新冠病毒感染者疾病严重程度及转归
“肠-肺轴”是肠道菌群紊乱后影响新冠病毒感染者的疾病严重程度及转归的重要机制。肠道是人体微生物最密集的区域之一,而下呼吸道是人体细菌最少的组织之一。虽然肠道和肺微生态环境和功能不同,但它们具有相同的胚胎起源和相似的结构。越来越多的证据表明肠道菌群紊乱与呼吸道感染相关,而肠道微生物菌群的健全与否又关系到包括肺在内的其他器官或组织的状态。这种肠道和肺之间的相互作用模式称为“肠-肺轴“。肠⁃肺轴是双向的,这意味着当肺部发生炎症时,内毒素和微生物代谢产物可以影响肺部,同样会影响肠道的微生物菌群。而肠道微生物菌群紊乱将促进Th17细胞极化,IL-17分泌增加,募集更多的中性粒细胞在局部聚集,释放细胞因子通过血液循环到达肺部,进一步加重肺部炎症。
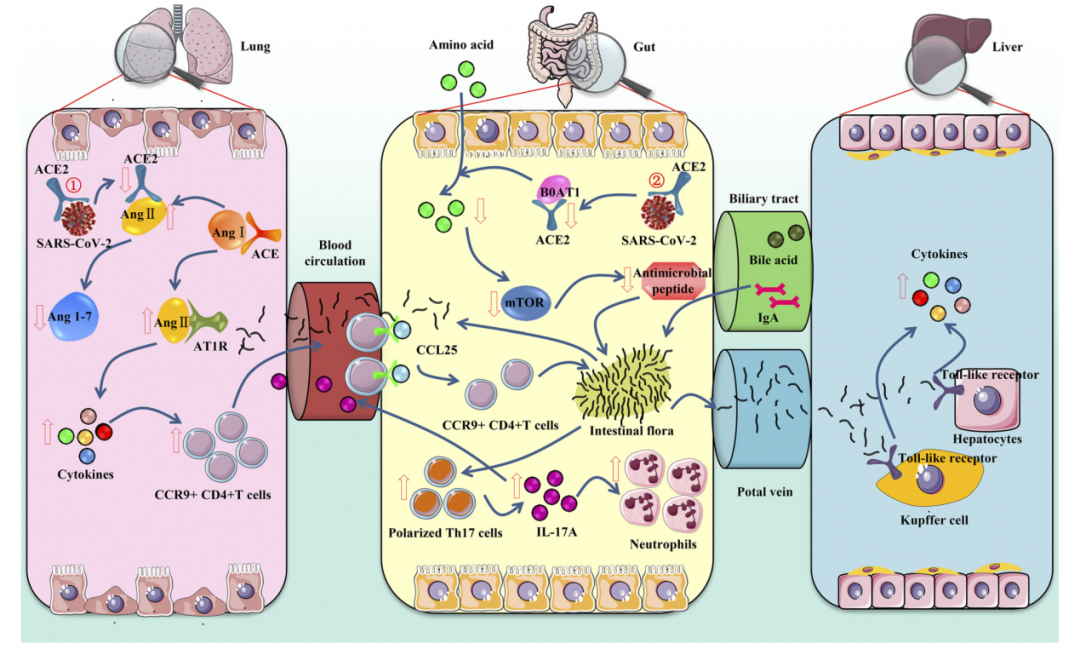
图4 肠道菌群紊乱对呼吸道感染的影响(“肠-肺轴”)
研究显示,新冠病毒感染者肠道微生物菌群发生位移改变,增加菌血症发生风险。而细菌感染又进一步增加肠道微生物菌群紊乱,从而形成恶性循环。
胃肠道症状的出现可能间接地反映患者的感染程度。研究显示,出现腹泻等胃肠道症状与新冠病毒感染者疾病严重程度显著正相关。此外,伴有胃肠道症状的新冠病毒感染者需要接受治疗的时间更久,且随着疾病严重程度的发展,胃肠道症状也更为严重。
四、新证据:益生菌在新冠病毒感染者中的应用探索
通过调节肠道菌群可以提高患者的免疫力,进而发挥抵抗细胞因子风暴的作用。近期不少研究为益生菌在新冠病毒感染者中的临床应用提供了循证医学证据。
国内学者早在新冠疫情暴发初期即评估了益生菌对重症/危重症新冠病毒感染者细胞因子水平的影响。结果显示,与对照组相比(仅接受常规治疗),经益生菌治疗后可显著降低新冠病毒感染者的细胞因子水平,提示经益生菌治疗后,有助于预防细胞因子风暴的发生,降低急性呼吸窘迫综合征发生风险。
西班牙学者进行的一项随机、双盲临床研究中,纳入300例门诊治疗的轻型新冠病毒感染患者,随机分为益生菌治疗组和对照组,两组均接受常规治疗。结果显示,治疗30天后,益生菌组完全缓解(病毒清除+5项核心症状完全消失)率显著高于对照组(53.1% vs. 28.1%, P<0.0001) ,且益生菌组患者发热、咳嗽、头痛、呼吸短促、肢体疼痛、呕吐、腹泻、稀便症状消失时间显著短于对照组。此外,治疗15天时,益生菌组病毒载量水平、高敏C反应蛋白、D-二聚体水平及胸部X线影像学评分即显著低于对照组,而新冠病毒特异性抗体水平显著高于对照组。
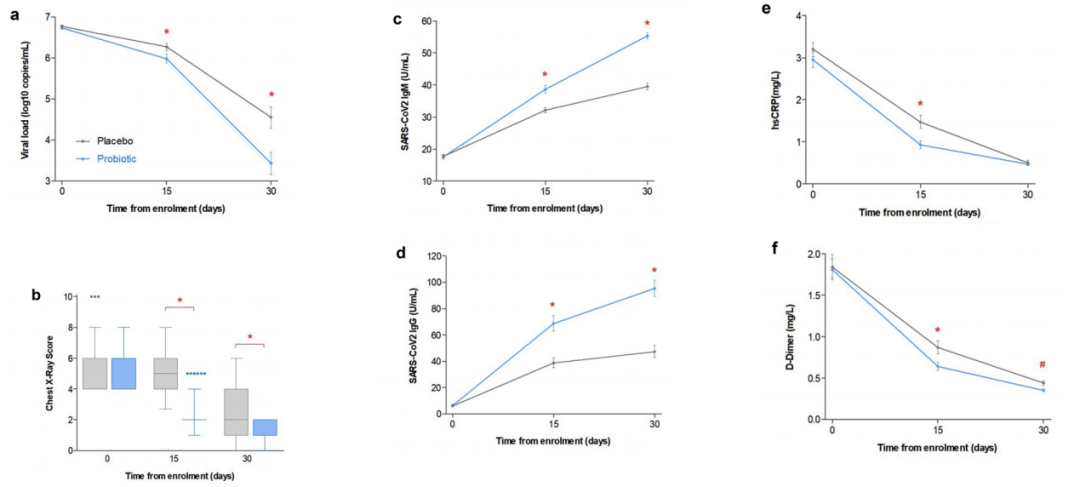
图5 益生菌组与对照组治疗期间病毒载量
(a)胸部X线影像学评分;(b)新冠病毒IgM抗体;(c)IgG抗体;(d)高敏C反应蛋白;(e)D-二聚体(f)水平改变
此外,益生菌对于预防新冠病毒感染亦有一定的潜在应用价值。PROMAGEN研究为一项随机双盲、安慰剂对照研究,纳入220例BMI为25~34.9kg/m2的健康成人,随机接受益生菌或安慰剂治疗,评估益生菌治疗对发生病毒性上呼吸道感染的预防作用。结果显示,为期6个月的研究期间,与安慰剂相比,益生菌可显著降低高BMI人群上呼吸道感染发生风险达27%,而在≥45岁及更高BMI(≥34.9kg/m2)人群中更为明显,上呼吸道感染风险降低达40%和43%。此外,该研究显示,治疗2周后,两组人群上呼吸道感染发生率即存在明显差异。

图6 益生菌治疗显著降低上呼吸道感染发生风险
五、新尝试:益生菌在新冠病毒感染者中应用价值探讨
肠道菌群的平衡有助于维持宿主免疫功能,为新冠病毒感染者防治提供新的途径。
预防新冠感染:已有研究显示,经益生菌治疗2周左右即可显著降低病毒性上呼吸道感染发生风险。益生菌不失为预防新冠病毒感染的有效措施,后续有待进一步研究加以证实。
轻症患者的治疗:研究显示,益生菌可显著改善轻症新冠病毒感染者的病毒清除率,加速症状缓解时间。
重型/危重型患者的治疗:李兰娟院士建议采用“四抗二平衡”综合措施调节肠道菌群平衡的方法治疗新冠病毒感染者,并强调其在危重病人的治疗中有重要作用。李兰娟院士指出,重症患者的肠道微生态通常是无序的,医务人员应采取维持微生态平衡的治疗手段,保持良好的肠道营养,补充微生态调节剂,结合中药治疗以减少继发感染引起的细菌转移。而《新型冠状病毒肺炎诊疗方案(试行第九版)》同样指出,对于重型和危重型患者,建议使用肠道微生态调节剂维持肠道微生态平衡,预防继发细菌感染。